药明生基AAV瞬转标准化工艺平台,专利高产包装系统,赋能全球AAV疗法2023年8月31日
腺相关病毒载体(Adeno-Associated Virus,AAV)属于细小病毒科依赖病毒属,直径20-26nm,是二十面体的微小无包膜病毒。AAV具有安全性高(主要以附加体形式存在),不整合基因组,免疫原性低,可长时间表达,转染效率高,且十余种血清型可靶向特定组织和器官,单次治疗长期疗效等多种优势,因此成为体内基因治疗递送的首选,以AAV载体为代表的新一代精准基因疗法给一些遗传性罕见病、神经系统退化性疾病、眼科疾病的治疗带来了新的希望。目前全球已上市的AAV药物共有6 款,中国AAV 市场更是呈现快速增长趋势,从2019年开始陆续有临床申报到目前已有25 款AAV药物的临床试验申请(IND)获批。
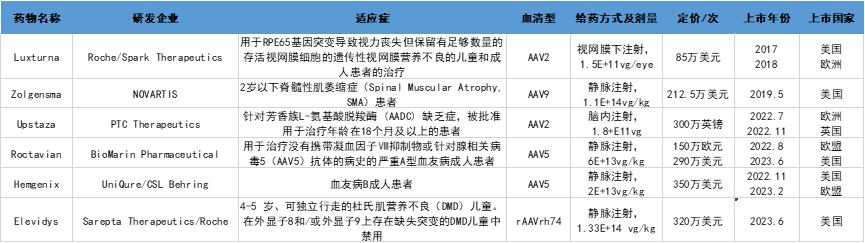
Fig1. 全球已上市的AAV药物汇总。来自公开资料整理
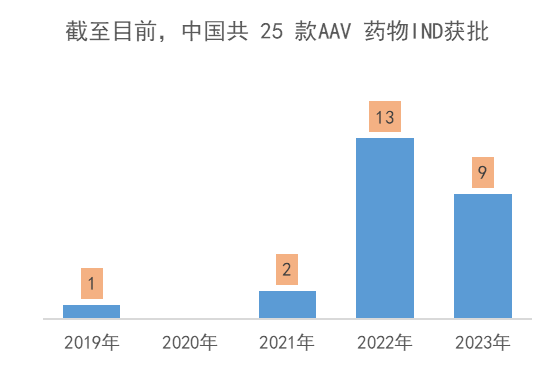 Fig2. 截止2023年8月,中国AAV 药物IND 获批情况。来自CDE官网和公开资料整理 01 AAV 工艺开发和商业化生产挑战
如图1,AAV 药物一般通过静脉注射或定点注射达到治疗效果,用于全身性治疗的AAV 药物用量较大,大规模生产时常使用基于HEK293 细胞的三质粒瞬时共转染悬浮系统,已上市的AAV药物中有3款均使用该系统,但该系统在工艺开发和商业化生产上面临以下挑战:
物料控制:起始物料细胞库、细胞库的构建到生产物料的选择以及生产过程中需要严格遵循法规指南生物安全性要求;
上游工艺:细胞系选择和授权、细胞与培养基适配性、转染用质粒比例影响滴度和空壳率等、转染复合物混匀等。病毒的产量和滴度取决于细胞系、质粒包装系统及生产工艺,空壳病毒以及错包病毒难以控制;
下游工艺:生产相关杂质如HCD/HCP/配基/核酸酶残留、产品相关杂质如不完整/错包/空壳病毒/rcAAV 等残留;
工艺放大:悬浮瞬时转染工艺操作复杂,放大困难,批间一致性差,使用的转染试剂、质粒和下游的纯化层析填料成本昂贵;上下游工艺放大稳定性;设备和产毒稳定性;
过程控制:AAV 载体对剪切力、pH、温度、离子强度等比较敏感,病毒易失活,目前没有有效及时的滴度检测方法;
成本高、商业化产能不足:预测AAV 到2030年需求1020 级别,目前200L AAV 的生产仅在1016 级别。
面对快速发展的AAV市场和不断增长的市场需求,通过创新和工艺优化突破生产瓶颈,实现AAV载体的高产和成本降低是关键的突破点。
02 关键起始物料优化——专利高产包装系统,滴度提升 ~8 倍
在rAAV生产工艺开发和生产过程中,上游的质粒转染步骤是获得高产量rAAV的关键,转染中所用的细胞系和包装质粒是决定病毒产量和滴度的关键起始物料。
药明生基AAV瞬转平台使用具有自主知识产权的稳定高性能的HEK293 细胞株,细胞活率高,一致性好,细胞库已检定放行,符合中美双报要求;包装质粒方面,通过对Rep 和Cap 包装质粒进行序列优化,让每个基因均衡表达,显著提升rAAV的产量和质量,实现rAAV 滴度 ~8 倍提升和感染效率显著提升(Fig3)。细胞库和不同级别AAV不同血清型高效病毒包装质粒现货供应,有效缩短项目研发周期。
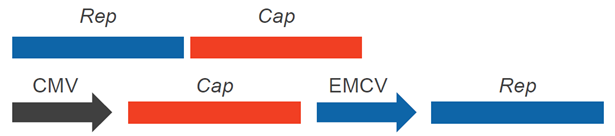 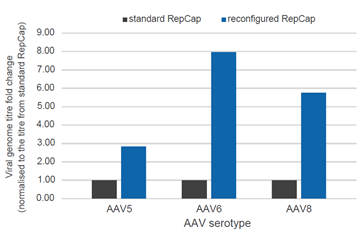 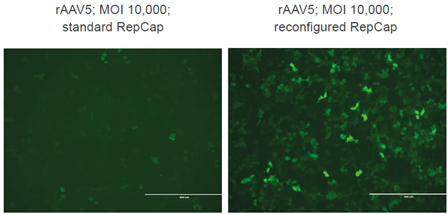
Fig3. 药明生基AAV包装质粒经序列优化后,AAV滴度和感染效率显著提升
03 上游关键工艺参数DoE优化——滴度提升4~5 倍
药明生基AAV 瞬转平台采用成熟的、自动化全封闭的悬浮无血清生产技术,生产规模最高达500L。通过自动化全封闭技术降低人工操作,提高工艺控制能力和工艺稳健性。针对不同产品开发建立多种工艺路径,通过DoE(Design of Experiment)进行关键步骤研究,风险评估确定关键工艺参数(Critical Process Parameters, CPP)和设计空间(Design Space),快速优化上游工艺参数,短时间内获得最优的工艺条件,实现生产效率显著提升。
药明生基通过Ambr®250HT 高通量生物反应器和MODDE® 实验设计软件快速优化rAAV 上游参数,可短时间内获得最优的工艺条件。上游工艺通过对细胞株、培养基、补料、转速、细胞密度、DNA用量、转染试剂TXF进行工艺开发和优化,获取更有助于病毒生产的工艺参数组合,提升AAV上游滴度和产量。在更换细胞、培养基和转染工艺参数等条件下,可实现滴度提升4~5 倍。
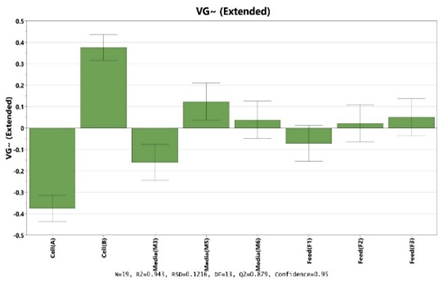 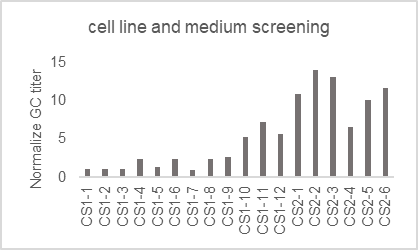
Fig4. AAV上游工艺参数优化——细胞株、培养基、补料
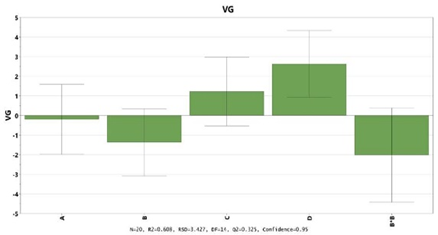 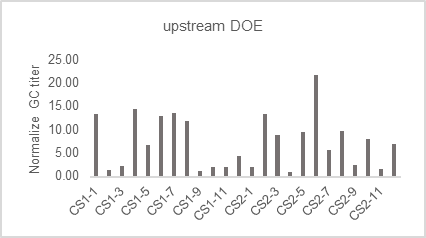 Fig5. AAV上游工艺参数优化——转速、细胞密度、DNA用量、转染试剂TXF
AAV要实现规模化生产,稳定的、易放大的生产体系是工艺开发的重点之一。药明生基标准化、可放大的AAV工艺平台,基于DoE 优化的工艺参数,可稳定放大至200L,在不同规模下细胞生长及AAV 表达单位滴度具有高度的一致性。
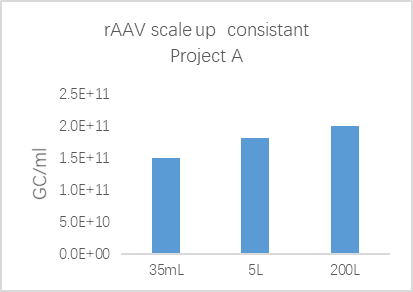 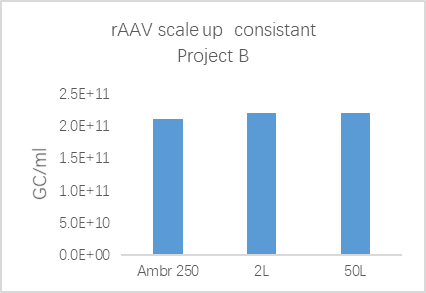 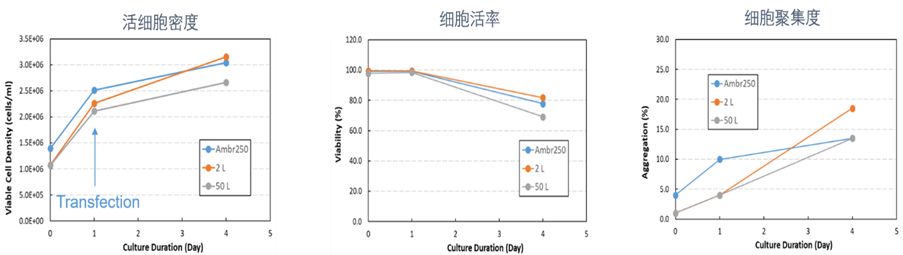
Fig 6. 从DOE 到200L 的工艺放大一致性
04 高收率rAAV 关键——易放大和经济的下游纯化工艺
AAV下游需经细胞裂解、核酸酶处理后,再进行澄清、层析、超滤、除菌过滤、及灌装等步骤。下游的生产挑战主要是生产相关杂质和产品相关杂质的残留,如HCD/HCP/配基/核酸酶,不完整/错包/空壳病毒/rcAAV 等。
药明生基采用易放大和经济的下游纯化工艺,如使用罐内裂解、低吸附高载量的深层过滤、亲和层析基于流速/缓冲液/层析填料载量等条件摸索等。通过对纯化工艺的条件摸索及多种纯化手段组合整体提升rAAV 载体的产率、降低杂质残留和纯化成本。药明生基GMP 级别下游纯化平台可达500L 生产规模,纯化后AUC 检测实心率高达90%以上。
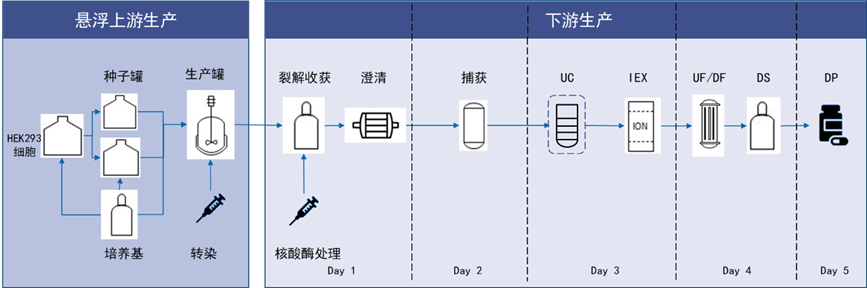 Fig 7. 药明生基AAV 瞬转平台工艺 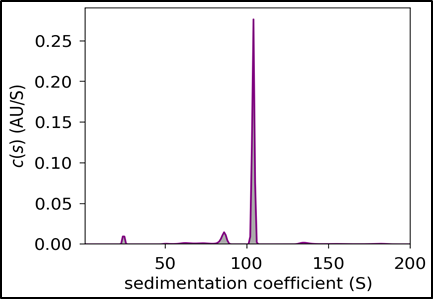 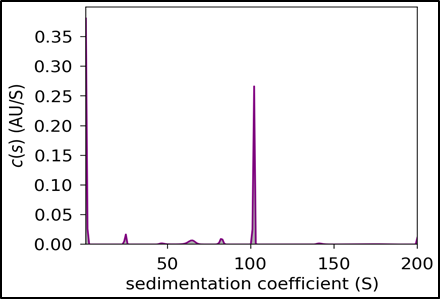 Fig 8. 终产品AUC 检测实心率
药明生基双平台,赋能全球 AAV 疗法
药明生基具有AAV三质粒瞬转系统和TESSATM (Tetracycline-Enabled Self-Silencing Adenovirus) 创新型下一代生产系统双技术平台,瞬时系统适合早期研发制备和小品种生产,TESSATM 系统适合中到大品种生产,满足客户从药物研发到商业化生产的不同阶段的需求。
三质粒瞬时转染系统采用具有自主知识产权的高性能稳定细胞株HEK293 及现货供应包装质粒,平台工艺标准化,适用于不同血清型AAV,缩短开发周期;成熟的悬浮工艺(无血清)生产技术易于放大,无动物源无抗生素,降低了生物安全风险,自动化封闭式工艺易于监控,工艺稳健且控制能力高。完善的质量控制和质量保证体系,确保产品安全有效;全面的分析检测方法能力,满足从研发到上市整个药品生命周期检测需求。
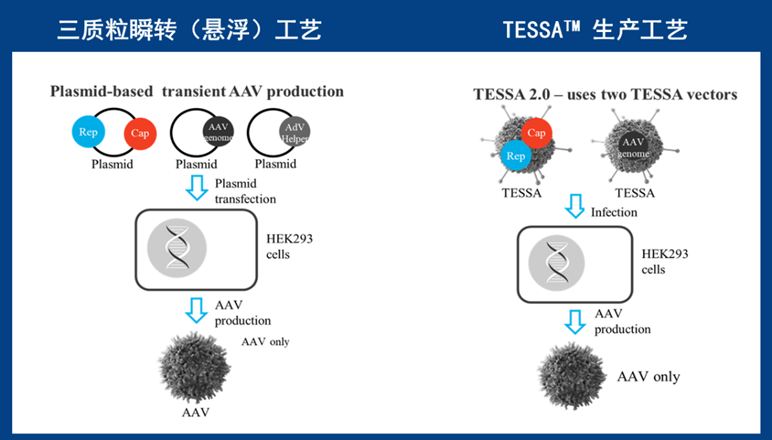 Fig 9.药明生基AAV 质粒瞬转平台和创新型下一代生产系统TESSA™
药明生基持续加强细胞及基因疗法CTDMO服务平台建设,截至 2023 年第二季度,为总计69个项目提供工艺开发、检测与生产服务,包括7个临床III期项目(其中2个项目处于上市申请审核阶段,2个项目处于上市申请准备阶段),10个临床II期项目,以及52个临床前和临床I期项目。2023年上半年,公司已助力客户完成一个将成为世界首个创新肿瘤淋巴细胞疗法(TIL)项目的FDA上市许可申请(BLA);以及助力客户完成一个CAR-T细胞治疗的慢病毒载体(LVV)项目的BLA,成为中国首家通过国家药品监督管理局食品药品审核查验中心(CFDI) LVV注册现场核查的CGT CDMO。
关于药明生基
药明生基是药明康德旗下专注于细胞和基因疗法的CTDMO (Contract Testing, Development and Manufacturing Organization),致力于加速和变革细胞和基因疗法及其他高端疗法的研究、开发、测试、生产和商业化。药明生基能够助力全球客户将更多创新疗法早日推向市场,造福病患。更多信息,请访问www.wuxiatu.com。
|
