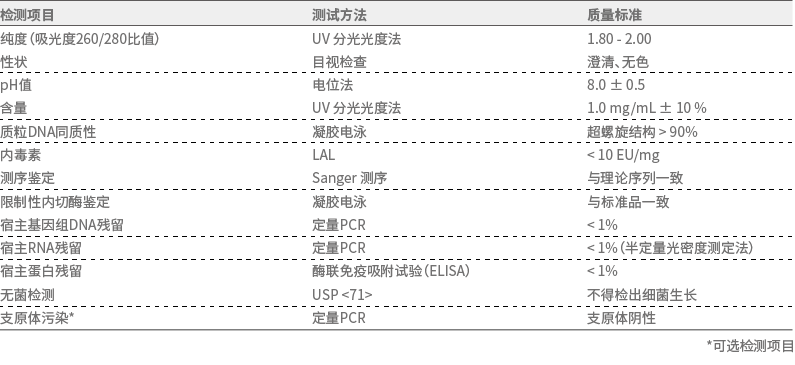
我们可提供药物主文件(DMF)授权信或质粒生产综述报告,加速您FDA的IND/BLA申报进程。同时,我们可将CTD格式模块3资料提供给CDE加速申报进程。我们的测试方法已依据ICH和其他法规指南进行了全面验证。
我们全程采用无抗生素生产工艺,这一点受到药品监管机构的高度青睐。无需额外检测和监控抗生素残留水平。使用不含任何动物组织成分的原料和一次性生物反应器及耗材,使微生物污染得到全部控制。
我们的质粒技术拥有超过25项全球专利申请。无论在研发、临床还是商业化阶段使用我们的质粒一概免授权费。

| 质粒类型 | 产品货号 | 描述 | 包装规格 |
| LV质粒 | AQ6972, AQ6973, AQ6975 | Rev、VSVG、GagPol | 1mg, 10mg |
| AAV质粒 | AQ1364 | AAV Helper | |
| AQ6587 | AAV1 Rep-Cap | ||
| AQ6801 | AAV2 Rep-Cap | ||
| AQ6589 | AAV3 Rep-Cap | ||
| AQ6802 | AAV4 Rep-Cap | ||
| AQ5220 | AAV5 Rep-Cap | ||
| AQ6961 | AAV6 Rep-Cap |
 立即点击订购
立即点击订购
